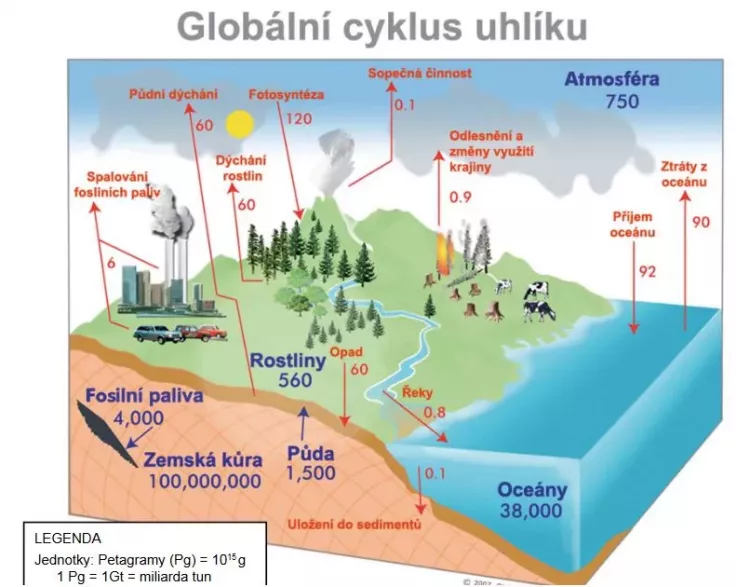
Od nejvyšší sekvoje přes nejchytřejšího člověka a nejjedovatější houbu až po tu nejmenší bakterii… existuje jedna věc, která spojuje vše živé na Zemi – skutečnost, že život je založen na uhlíku. To, že se jedná o významný chemický prvek, dokazuje i fakt, že se jím, zjednodušeně řečeno, zabývá jedna celá oblast chemie, a to ta organická.
Výjimečnost uhlíku
Uhlík ovšem není nejrozšířenější prvek, tím je kyslík, a zároveň není ani nejstabilnější jako například helium. Na první dojem se tedy nezdá výjimečným, avšak při podrobnějším zkoumání složení našeho těla zjistíme, že 20 % buněk lidského organismu je tvořeno uhlíkem. Otázkou zůstává, proč tomu tak je. V celkovém měřítku totiž uhlík představuje méně než 1 % hmotnosti zemské atmosféry a zemské kůry. K dispozici jsou i hojnější kyslík, křemík nebo dusík, který tvoří dokonce 78 % atmosféry. Z jakého důvodu si tedy příroda při výběru složení organismů vybrala právě uhlík?
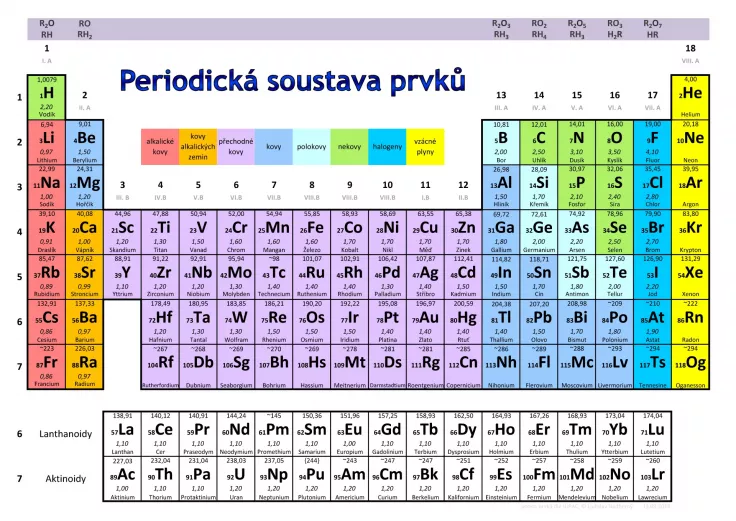
Periodická tabulka prvků čítá 118 prvků, z nichž přes 90 se přirozeně vyskytuje na Zemi a zbylé byly vytvořeny uměle. Proč je tedy tak důležitý právě uhlík? Odpověď zahrnuje tři základní aspekty – složitost, hojnost a stabilitu.
Z hlediska zmíněné složitosti je uhlík schopen vytvářet složité molekulární struktury potřebné pro komplexní sloučeniny, které jsou nutné pro život. Abychom pochopili, proč je toho uhlík vůbec schopen, je nutné podívat se na základ chemie, kterým je fyzika, zejména kvantová mechanika. Ta říká, že některé konfigurace elektronových orbitalů (prostorové rozložení možného výskytu elektronu kvantového stavu v elektronovém obalu atomu) jsou energeticky výhodnější než jiné, což je činí stabilnějšími. Mezi nejstabilnějšími konfiguracemi elektronů jsou konfigurace vzácných plynů na pravé straně periodické tabulky. Jde o speciální prvky, které mají vnější slupku plnou elektronů, což je konfigurace s nejnižší energií, kterou může atom mít, a to je činí chemicky stabilními. K tomu, aby vytvořily vazby s jinými atomy, nepotřebují totiž získávat nebo odbourávat elektrony. Jsou tedy chemicky inertní, neinteragují s ostatními atomy a netvoří molekuly.
Tyto vlastnosti vykazují pouze vzácné plyny, které mají vhodný počet protonů k tomu, aby došlo k zaplnění jejich slupky elektrony. Podstatou chemie je právě dojít k energeticky nejefektivnějšímu stavu, tedy ke stavu s nejnižší energií, jako je tomu u vzácných plynů. Periodická tabulka prvků je uspořádána tak, že můžeme snadno určit podle sloupce maximální počet vazeb, které může prvek vytvořit s jinými prvky – počínaje levým sloupcem tabulky první skupina atomů je schopna vytvořit maximálně jednu vazbu, druhý sloupec prvků může vytvořit dvě vazby a třetí sloupec tři vazby. Toto pravidlo pokračuje až do čtvrtého sloupce, který může vytvořit čtyři vazby, a poté se maximální počet vazeb snižuje, takže pátý sloupec prvků vytvoří maximálně tři vazby, poté dvě vazby, jednu vazbu a nakonec nulovou vazbu pro sloupec vpravo, což jsou ušlechtilé prvky, které jsou nejstabilnější.
Všestranný uhlík a jeho nevýhoda
Uhlík patří do skupiny prvků, které mohou vytvářet maximální počet vazeb. Jeho atomové číslo je šest, má tedy celkem šest protonů a šest elektronů, z nichž čtyři jsou v jeho druhé, tedy valenční slupce. Aby se stal stabilním, musí zaplnit svoji vnější slupku dalšími čtyřmi elektrony. Ke stabilitě potřebuje totiž dohromady osm elektronů. Díky tomu je uhlík velmi všestranný. Představte si, že by kostky Lega mohly být spojeny na čtyřech stranách místo dvou, skládání by tak bylo jednodušší. Jak jsme již zmínili, každý atom uhlíku může vytvořit silnou stabilní vazbu až se čtyřmi dalšími atomy, a to včetně jiných atomů uhlíku. Tato vlastnost mu umožňuje vytvářet složité molekuly, což je nezbytné pro složité chemické reakce, které život vyžaduje. Molekuly na bázi uhlíku mohou tvořit dlouhé neopakující se řetězce polymerů, uzavřené kruhy a mohou vytvářet jednoduché dvojné nebo trojné vazby s jinými prvky. Celkem existují miliony možných konfigurací, díky čemuž je uhlík schopen účastnit se obrovského množství chemických procesů.
Mimo jiné může snadno vytvářet dlouhé stabilní polymerní řetězce, které mohou nést například velké množství informací nebo čtyři nukleotidy, což je stavební kámen DNA. Koneckonců může nést všechny informace, které tvoří živé organismy včetně člověka. Uhlík je významný právě proto, že je schopný zvládat tyto složité koncepty. Například nejrozšířenější kyslík může tvořit pouze dvě vazby, může se spojit maximálně s dvěma atomy. Nevýhodou uhlíku je jeho extrémní vzácnost, není pro život, kterého je ale vlastně základem, snadno dostupný. To nás přivádí k druhému faktoru, který učinil uhlík atraktivním, a tím je právě hojnost.
Navzdory malému podílu uhlíku v zemské atmosféře je ale možné uvést, že je zastoupen poměrně hojně. Pokud se zaměříme na pět nejrozšířenějších prvků ve sluneční soustavě, dle jejich zastoupení vyjmenujeme vodík, helium, kyslík, uhlík a dusík. A pět nejrozšířenějších prvků v našem těle jsou kyslík, uhlík, vodík, dusík a vápník. Tedy čtyři z pěti nejrozšířenějších prvků sluneční soustavy je také mezi pěti nejrozšířenějšími prvky, které tvoří lidské tělo. To nám přináší další důvod, proč je život založen na uhlíku. Ve vesmíru je ho dostatek, jeho hojnost je velmi vysoká. Možná se ptáte, proč není tak významný například křemík, jehož zastoupení je taky dostatečné a současně zvládne tvořit až čtyři vazby. To nás dovádí ke třetímu faktoru, který příroda vybrala pro stabilitu života.
Pevná uhlíková kostra
Třetím aspektem je stabilita vazby. Jak je zmíněno výše, struktura periodické tabulky je taková, že zpravidla všechny prvky v každém sloupci mají stejné obecné vlastnosti. Uhlík je nejlehčí prvek ve své skupině. Dalo by se tedy očekávat, že sousední prvky jako křemík nebo germanium budou vykazovat podobné chemické vlastnosti. Například právě křemík je opravdu dalším nejlehčím prvkem ve sloupci. Jeho umístění v periodické tabulce nám říká, že stejně jako uhlík má také čtyři valenční elektrony, což znamená, že může taktéž vytvářet čtyři kovalentní vazby. Zároveň je křemík na Zemi také poměrně hojně zastoupen, dokonce ho je víc než uhlíku. Je ale obsažen v horninách v zemské kůře. Chemicky má křemík čtyři nespárované elektrony ve vnějším orbitalu stejně jako uhlík, ovšem hlavní rozdíl spočívá v tom, že křemík má nespárované elektrony dále od jádra ve své třetí slupce, zatímco elektrony uhlíku jsou ve druhé slupce blíže k jádru. To způsobuje, že elektrony křemíku jsou na jeho jádro vázány slaběji proto, že v případě, kdy se křemík váže na jiné atomy včetně svých vlastních, jsou vytvořené vazby slabší, a tedy méně stabilní. Tento faktor pevnosti je také důvodem, proč se například dusík, jehož zastoupení v atmosféře je velice výrazné, příliš nehodí jako základ organické chemie. Pevnost jeho vazby je totiž přibližně poloviční ve srovnání s uhlíkem.
Nelze postavit dům, aniž by byla konstrukce pevná a stabilní. Podobně výstavba molekul musí být dostatečně silná, aby vydržela podmínky, kdy ostatní části molekuly narušují své vazby a chemicky reagují s jinými molekulami. Uhlíková kostra musí zůstat neporušená, zatímco některé složky se rozpadají. Kostra dusíku nebo křemíku by se rozpadla poměrně snadno. Pokud tedy opět odkážeme na periodickou tabulku prvků a odstraníme inertní prvky, prvky s neschopností tvořit více než dvě vazby a prvky s mimořádně malým zastoupením, skončíme u uhlíku, dusíku a křemíku. Následně odstraníme ty, které nemohou tvořit silné jednoduché vazby a nevytvoří tak silnou molekulární páteř. Jako nejlepší volba tedy zůstává pouze uhlík. Je jedinečně vhodný pro život, a to díky nejlepší kombinaci schopnosti tvořit složité struktury a stabilní vazby s ostatními atomy uhlíku.
Přežije uhlík všechno?
Co se jeví jako možná nevýhoda, je snadné rozbití polymerních řetězců uhlíku. Ovšem, a bohužel se to nemusíme nikdy dozvědět s jistotou, uhlík může přežít veškeré podmínky jen kromě nadmíru extrémních. Je stále na místě být otevřený a zkoumat podmínky, ve kterých by se hypoteticky mohl vyskytnout život. Například na měsíci Titan jsou jezera etanu a metanu. V rámci zdejších podmínek se jedná o kapaliny, podobně jako voda na Zemi by tedy mohly být použity jako základ pro jinou formu života. Zkrátka je v případě odlišných teplot možné, že jiný prvek v takových podmínkách může být ve srovnání se Zemí pro život příznivý. Například můžeme poukázat na to, že lidské organismy jako uhlíkové formy života mohou být aktuálně v procesu vytváření křemíkových umělých forem života, jejichž vznik by mohl být záležitostí blízké budoucnosti, a to dokonce zde na Zemi. Tím, že neexistují žádné důkazy o životě mimo naši planetu, by takový typ života byl vzácný.
Chemické interakce různých prvků představují kritický proces, avšak potřebný pro život. Pro pochopení, že tyto procesy jsou plně organickou chemií, je možné studovat i další materiály jako například kurzy jednoho z nejlepších pedagogů na světě, Rona Davise z Georgetownské univerzity.